报道
日前,FDA发布电子格式提交临床研究用新药安全性报告指南草案,
要求申办者在指南最终版发布24个月后,向FDA不良事件报告系统提交IND的严重和意外可疑不良事件安全报告
。做出这一规定的原因何在?具体涉及到哪些提交?

改变现行提交方式,改进审查、跟踪效率
按照现行要求,FDA要求这些报告都以PDF格式的电子通用技术文件提交。但对这些文件的审查和跟踪效率低下,耗费大量人力。因此,
FDA要求将这些重要的安全信息作为结构化数据元提交给FAERS,有助于提高 FDA 审查和跟踪临床试验期间发生的潜在安全信号的能力
,并为申办方提供符合ICH E2B要求以及向其它监管机构报告的要求报告格式。对相关提交要求的转变,是FDA具体落实《联邦食品、药品和化妆品法案》第745A节规定的电子提交要求工作的一部分。
FDA表示,申办方目前还可以继续通过eCTD提交相关的IND安全报告;但在要求生效之前,申办方可以自愿向FAERS提交报告。但最终版指南一旦生效,FDA将要求IND安全报告的提交符合新指南的规定,取代2019年1月颁布的《按照eCTD规范提交部分人用药品申请和相关提交》行业指南的相关规定。

依据指南规定,
申办方必须通过 FDA 的电子提交网关或安全报告门户 , 向FAERS 提交相关的 IND安全报告
。
通过FAERS提交IND安全报告所涉范围
新公布的指南草案,不适用于严重和意外疑似不良事件之外的IND安全报告
,诸如详细说明来自于其它研究的结果的报告,来自于实验动物或体外检测的结果,或严重疑似不良反应发生率增加的报告。此外,FDA表示,尽管FDA鼓励申办方以电子方式提交,非商业性IND的提交,将豁免第745A节规定的电子提交要求。
除了指南草案之外,作为指南草案的补充,FDA 还发布了单独的技术符合性指南,详细说明应以eCTD格式提交给FDA的个案安全报告 ,以及提交给 FAERS 的 IND 安全报告应采用的格式。
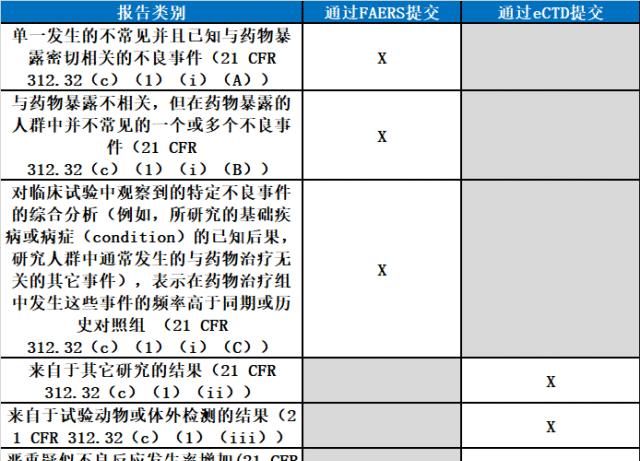
IND安全报告的类别与提交方式
FDA正在就这份指南草案征询医药行业和利益攸关方的建议与意见,征询日期截止于今年年底。
FDA新药审评程序包括新药临床试验申请IND申报和新药申请NDA申报两个过程,申请人在完成新药临床前研究后,便可向FDA提出IND申请,若FDA在收到后30天内未提出反对意见,申请人便可自行开展新药临......
2019年12月9日,药明巨诺中国(下称“药明巨诺”)今日在第61届美国血液病学会(ASH)年会上公布其首个在研产品JWCAR029治疗成人复发/难治B细胞非霍奇金淋巴瘤(R/RB-NHL)的I期临床......
昨日,Curis宣布,美国FDA已经接受了该公司产品CA-170的新药研究申请(IND)。总部位于美国马萨诸塞州莱克星顿的Curis是一家专注于人类癌症药物研究和开发的生物技术公司。CA-170是一剂......
创新药研发是一个探索性的研究过程,是由未知开始,基于未被满足的临床需求,开展药物筛选与发现的研究工作。因研发基础不同,创新药与仿制药具有完全不同的研发路径,因此其CMC申报也不相同。CMC指的是化学、......
时光飞逝,以前所学的专业知识似乎都还给老师了;还不到三年,初入职场时的兴奋与激情似乎在悄悄地淡去。。。 &......