作者:药渡
链接:https://www.zhihu.com/question/267087191/answer/318158551
来源:知乎
著作权归作者所有。商业转载请联系作者获得授权,非商业转载请注明出处。
创新药物从结构设计到发现、再到最终的获批上市,经历的是一个充满荆棘的系统的炼狱过程。简要的说,首先是新化学实体NCE的发现,其主要包括先导化合物、候选药物的确定;之后进入到临床前研究阶段,这一过程主要包括药理、毒理、药代、处方前研究等内容;待完成初步临床前评价后,即将进入临床研究之时,开发公司申请人须向相应药审部门进行注册申报,这个节点就是本文要讲的内容~IND申请;待药审部门通过IND申请或者没有反馈意见时,项目便进入到下一阶段,即I、II、III期临床研究;待临床前研究、临床研究全部或部分完成之后,如果达到了预期目的,即可提交新药上市申请NDA,以求获批上市销售;上市后,开发公司仍需对产品进行IV期临床研究和上市后监测,使之更加充分的理解药物的机理、范围、治疗作用、副作用,等等等等....
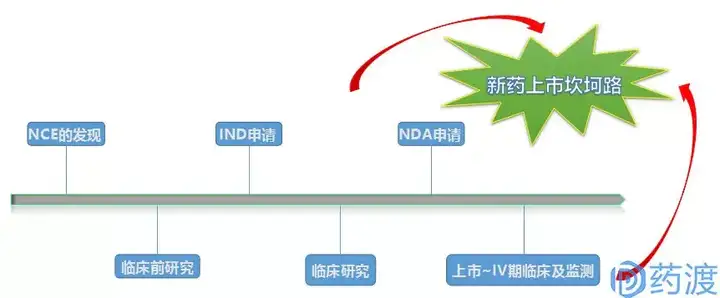
FDA新药审评程序包括新药临床试验申请IND申报和新药申请NDA申报两个过程,申请人在完成新药临床前研究后,便可向FDA提出IND申请,若FDA在收到后30天内未提出反对意见,申请人便可自行开展新药临......
2019年12月9日,药明巨诺中国(下称“药明巨诺”)今日在第61届美国血液病学会(ASH)年会上公布其首个在研产品JWCAR029治疗成人复发/难治B细胞非霍奇金淋巴瘤(R/RB-NHL)的I期临床......
昨日,Curis宣布,美国FDA已经接受了该公司产品CA-170的新药研究申请(IND)。总部位于美国马萨诸塞州莱克星顿的Curis是一家专注于人类癌症药物研究和开发的生物技术公司。CA-170是一剂......
创新药研发是一个探索性的研究过程,是由未知开始,基于未被满足的临床需求,开展药物筛选与发现的研究工作。因研发基础不同,创新药与仿制药具有完全不同的研发路径,因此其CMC申报也不相同。CMC指的是化学、......
时光飞逝,以前所学的专业知识似乎都还给老师了;还不到三年,初入职场时的兴奋与激情似乎在悄悄地淡去。。。 &......