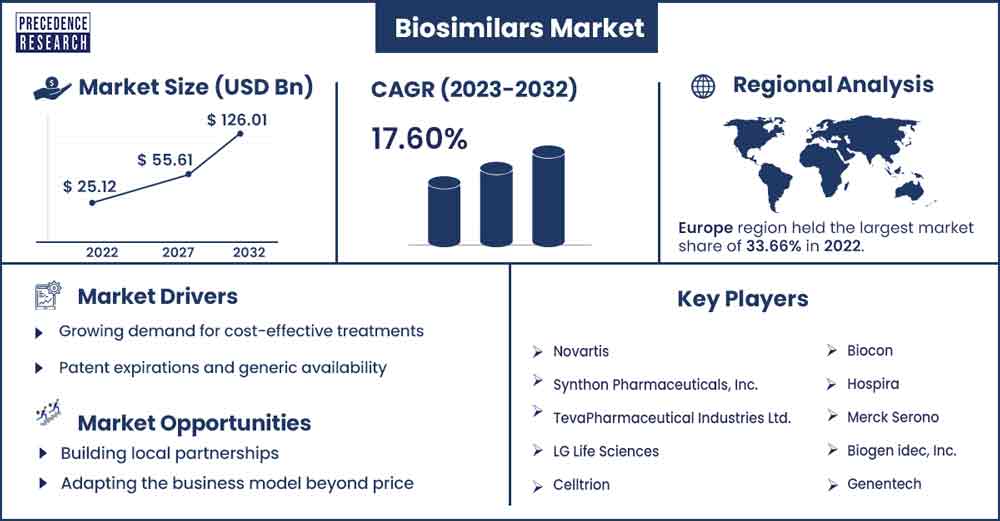
2022年全球生物仿制药市场规模为251.2亿美元,预计到2032年将达到1260.1亿美元左右,2023年至2032年复合年增长率为17.6%。
生物仿制药市场是生物制药行业的一个部门,专注于开发和生产与生物治疗高度相似的药物,称为生物制剂。生物仿制药的设计目的是与原始生物制剂具有相同的安全性、功效和纯度,但它们通常更便宜。这使得它们成为寻求经济高效治疗的患者和医疗保健提供者的有吸引力的选择。生物仿制药在免疫学、肿瘤学、支持治疗、眼科和糖尿病等治疗领域至关重要。
生物仿制药的一个关键方面是通过输注或注射进行给药。这种输送方法使它们能够用于各种治疗领域,有助于其不断增长的市场份额。此外,生物仿制药市场正在不断增长,因为它们能够提供具有成本效益的原始生物制剂替代品,增加治疗选择和患者可及性。它们需要经过严格的审批流程,以确保其安全性和有效性,在更广泛的医疗保健行业中发挥着关键作用。
欧洲是全球生物仿制药市场的主导地区。在欧洲,许多人正在采用生物仿制药,这是市场增长最重要的增长因素。监管机构在生物仿制药的采用中发挥着至关重要的作用。欧洲在生物技术领域拥有重要的创新和研究,这通常会导致生物仿制药等先进疗法的开发。增长因素之一是慢性病治疗的成本效益。人口中慢性病的增加以及许多国家和监管机构对大量生物仿制药的批准预计将迅速提高全球生物仿制药的接受度。人们对生物仿制药及其有效性的认识不断提高,也推动了全球对生物仿制药的需求。
这些生物仿制药的设计目的是与原始生物制剂具有相同的安全性、功效和纯度,但它们通常更便宜。尤其是肿瘤学领域,在生物仿制药市场占据主导地位,这主要是由于价格较低且癌症患者数量众多,这使得癌症治疗变得更加实惠和容易获得。这是欧洲等地区增长的另一个原因。
| 报告范围 | 细节 |
| 2023年市场收入 | 293.9亿美元 |
| 到 2032 年预计收入 | 1260.1亿美元 |
| 2023年至2032年增长率 | 年复合增长率为 17.6% |
| 最大的市场 | 欧洲 |
| 基准年 | 2022年 |
| 预测期 | 2023年至2032年 |
| 覆盖地区 | 北美、欧洲、亚太地区、拉丁美洲、中东和非洲 |
司机
对具有成本效益的治疗的需求不断增长
生物仿制药市场的主要驱动力之一是对具有成本效益的治疗的需求不断增长。患者和医疗保健系统都在寻找昂贵生物药物的替代品。生物仿制药与其原始生物制剂高度相似,可以在不影响安全性或有效性的情况下降低成本。这使它们对付款人和患者具有吸引力,为市场的增长做出了重大贡献。
专利到期和通用可用性
推动生物仿制药市场增长的另一个因素是许多生物药物的专利到期。专利到期后生物仿制药的可用性有助于维持这些基本治疗的使用,确保患者继续获得它们,即使原始生物制剂的成本可能发生变化。
监管进展和标准
生物仿制药的监管进步和标准的建立也对市场起到了推动作用。世界各地的监管机构正在制定指导方针,以确保生物仿制药符合与其原始生物制品相同的质量标准。这不仅让患者和医疗保健提供者放心,还为生物仿制药的开发和商业化创造了稳定的环境。
协作方法和战略伙伴关系
合作方法和战略伙伴关系在生物仿制药市场中变得越来越普遍。公司正在与药房、处方福利管理者 (PBM) 和其他利益相关者合作,提供他们的产品并展示他们的价值。这种合作模式使生物仿制药公司能够利用其合作伙伴的现有网络并覆盖更广泛的受众,从而加速生物仿制药的采用并推动市场增长。
限制
挑战和准入障碍
由于多种因素,在美国医疗保健系统中获取生物仿制药可能具有挑战性。由于系统的复杂性,提供商通常会遵守保险偏好,这可能会限制患者可用的选择。处方限制和保险范围问题产生了进一步的障碍,使得医疗保健提供者很难开出特定的生物仿制药。
由于商业保险限制而利用率不足
尽管生物仿制药具有诸多优点,例如与生物仿制药相比成本更低,但在许多情况下仍需要更多地利用它们。原因之一是商业保险限制,这可能会降低生物仿制药对医疗保健提供者和患者的吸引力。这些限制可能会限制患者可用的生物仿制药的选择,并影响这些产品的总体利用率。
复杂的开发流程
生物仿制药的开发过程很复杂,需要广泛的研究和验证。这对于进入市场的公司来说可能是一个重大障碍,因为他们必须在研发上投入大量资金以证明与参考生物制剂的相似性。高昂的开发成本和严格的监管要求可能会阻止新进入者并减缓生物仿制药的市场渗透率。
监管不确定性
监管不确定性可能会限制生物仿制药市场。尽管监管机构正在努力简化生物仿制药的审批流程,但对明确指南的需求可能会带来不确定性,从而延迟产品上市或增加成本。此外,不同司法管辖区的法规必须一致,以挑战生物仿制药产品的国际扩张。
机会
建立当地合作伙伴关系
对于新兴市场生物仿制药公司来说,建立当地合作伙伴关系是一项强有力的战略。与跨国公司相比,本土公司能够更好地了解市场并应对复杂的监管环境。他们还可以降低制造成本并利用当地知识。跨国公司可以与区域参与者建立合作伙伴关系来进入这些市场,从而实现快速渗透并建立与政府机构和客户的现有关系。
调整商业模式,超越价格
公司正在探索调整其商业模式的方法,而不仅仅是关注价格,以增加新兴市场的准入机会。这可能涉及增强生物仿制药价值主张的策略,例如改善患者治疗结果、简化给药过程或提供更方便的剂型。
2024年2月,全球最畅销药物修美乐(阿达木单抗,艾伯维)的九款生物类似药上市,提振了美国医药市场。
赛尔特龙
百康
霍斯皮拉
默克雪兰诺
百健艾迪公司
基因泰克公司
诺华公司
Synthon 制药公司
梯瓦制药工业有限公司
LG生命科学
市场细分
按产品分类
单克隆抗体
生长激素
胰岛素
促红细胞生成素
促卵泡素
其他的
按申请
肿瘤学
生长激素缺乏症
血液疾病
慢性及自身免疫性疾病
传染性疾病
其他的
按制造商
合同研究和制造服务
内部
国药现代(600420)3月7日晚间公告,近日,公司控股子公司国药集团致君(深圳)制药有限公司收到国家药监局核准签发的《药品补充申请批准通知书》,批准注射用头孢哌酮钠舒巴坦钠通过仿制药质量和疗效一致性......
2024年全国两会,全国人大代表、华海药业(600521)总裁陈保华带来两项议案与多项建议。针对医药行业,陈保华就药品专利期限补偿制度中增设“出口豁免”规定、新药参比制剂遴选政策、扩大国家集采的慢病药......
2022年全球生物仿制药市场规模为251.2亿美元,预计到2032年将达到1260.1亿美元左右,2023年至2032年复合年增长率为17.6%。市场概况生物仿制药市场是生物制药行业的一个部门,专注于......
近日,据CDE官网最新公示,正大天晴的1类创新药ATR激酶抑制剂TQB3015片获批临床(默示许可),用于治疗晚期恶性肿瘤。2023年至今,正大天晴药业集团共有4款抗肿瘤(化学或生物药)1类新药冲刺上......
仿制药是与原研药具有相同活性成分、剂型、给药途径和治疗作用的药品。在仿制药的质量和疗效一致性评价过程中,参比制剂的选择是关键环节之一。参比制剂是与原研药进行比较研究的标准物质,用于评估仿制药的质量和疗......
2018年以来,我国已开展8批国家组织药品集采,涉及333种药品。2021年6月起,国家医疗保障局委托首都医科大学宣武医院牵头对第二、三批国家组织集采的23个代表性品种,开展第二期临床疗效和安全性真实......
上周,上海阳光医药采购网官宣了第九批集采将于11月6日正式开标,本轮集采最大的特点就是部分品种集采结果要执行到2027年12月31日,也就是采购周期长达4年,为历次国采标期之最。截至目前,国家组织带量......
今天(17日),国家医保局召开新闻发布会,介绍第二、三批国家组织药品集中采购中选仿制药临床疗效和安全性真实世界研究结果。2021年6月,受国家医保局的委托,首都医科大学宣武院牵头全国16个省29家医疗......
近日“药茅”恒瑞医药(48.230, 0.91, 1.92%)(600276.SH)2022年年报出炉,报告期内营收、归属净利润均双位数下降,这也是继2021年之后第二年“双降”。......
药企之间,是有鄙视链的:做FirstinClass/BestinClass的看不起做Mebetter的;做Mebetter的看不起做Metoo的;做创新药的看不起做仿制药的。在这条鄙视链里,仿制药沦为......