超高速测序推动基因组诊断快速发展
简化的DNA和RNA测序工作流正在帮助临床医生在几天甚至几小时内提供迅速的有针对性的护理
约十年前,澳大利亚墨尔本的默多克儿童研究所的临床遗传学家Zornitza Stark等研究人员着手探讨基因组测序如何改善婴儿护理。研究中,他们发现了一个能够解释神经症状的遗传变异,但从采样到得到答案竟花费了六个月,使得治疗时效性大打折扣。
如今,超高速测序技术的涌现改变了这一局面。该技术能够在一周内提供诊断结果,甚至在一小时内对肿瘤进行分类和制定治疗计划。技术进步之快,即使对于早期采用者也可能难以跟上。圣地亚哥的雷迪儿童基因医学研究所的快速测序先驱Stephen Kingsmore表示:“大约每18个月,我们都会经历一次技术革命——不是演变,是革命。”[1][2]
突破瓶颈
测序数十亿个核苷酸,以足够的“冗余”确保高精度结果需要时间,而检查结果以识别潜在相关序列异常则需要更长时间。即使是更为有针对性的“外显子”分析,它关注的是包含蛋白质编码基因的基因组的1-2%,也需要几个月的时间来提供答案。
2012年,圣地亚哥的测序公司Illumina联系到当时他所在的机构——密苏里州堪萨斯城的儿童慈善医院,以测试其新的“快速运行模式”。Illumina是短读取测序的市场领导者,该过程产生数十亿个100-200核苷酸的DNA序列“读数”,然后可以通过计算重新组装成整个基因组或外显子。这种模式结合了测序化学和分析的进展,使测序步骤从约10天减少到1天。Kingsmore和他的同事建立了一个围绕新模式的诊断工作流程,允许他们在采集血样后的50小时内确定新生儿的可能致病突变。[3]
“我们解码基因组的前四例中有三例发现了结果,就像炸弹爆炸了一样,”Kingsmore说。从那以后,他一直在完善这个过程,发表了数十篇研究论文,并协调了一个名为Baby Bear的试验,该试验在2018年至2020年间在加利福尼亚的5家医院中展示了实施这种诊断工作流程的可行性,涉及近200名婴儿。他估计,每年有数千名美国儿童接受这项服务。

Ultra-rapid sequencing of human genomes can identify rare diseases and speed up treatment. Credit: Jean-Philippe Ksiazek/AFP/Getty
测序仪器也变得更快了。许多实验室使用Illumina的最先进的NovaSeq X Plus,它每天可以产生数万亿个核苷酸的测序数据。但这可能会很昂贵——这种高通量系统的经济优势在一次处理多个样本时才会显现。但大多数快速测序样本代表紧急的个体病例,因此进行测序的成本与在更高效的工作流程中处理数十个基因组的成本一样高。
另一个有助于的因素是不断发展的计算工具。初步的基因组处理和分析现在可以使用基于云的资源进行,这样可以避免研究人员使用昂贵的高性能计算机。而软件包也已经发展到可以自动化关键的分析步骤。Kingsmore和Abou Tayoun都在使用Illumina的DRAGEN工具包,以快速收敛到相关的序列和结构变异,例如。还有一些有用的资源,如GeneMatcher,这是一个在线服务,帮助世界各地的遗传学家和临床医生交换有关与疾病相关的突变的见解。在使用GeneMatcher帮助诊断一名年轻患者的几分钟内,Baple的团队就与其他患有一种叫做扩张型心肌病的心脏病的儿童的相似突变的报告联系上了。“扩张型心肌病的记录意味着孩子在足够大的时候有可能进入移植名单,”她说。
然后是人工智能(AI)的承诺。Abou Tayoun估计,遗传学家和其他专业人员在首次诊断交付之前大约需要一个小时来手动审查每个基因组。但是AI的能力正在成熟,Kingsmore预测这种技术将很快产生重大影响。AI系统“确实会错过一些事情,他们确实会犯错误,但你现在可以在10分钟内对基因组进行解释,”他说。与此同时,“我们仍然需要大量的人力参与”。
展望长远
Illumina仍然是全球几乎所有临床测序项目的支柱,但它面临着许多竞争对手。尽管这些平台仍然太新,没有实质性的临床记录,但它们可能使无法负担NovaSeq X Plus的单一样本分析的用户能够使用高于100万美元的价格标签。
Kingsmore对来自圣地亚哥的Element Biosciences的AVITI仪器特别感兴趣。该仪器设计用于中等吞吐量,并且具有公司声称与或优于Illumina的基础准确性的每碱基准确度。“你购买三台仪器——而且这些仪器相对便宜,每台约25万美元——你就能得到200美元的基因组,”他说。相比之下,仅仅十年前对整个基因组进行测序的成本大约是10000美元。“这将是非常具有变革性的。”
但也许最令人兴奋的是“长读取”技术,特别是由英国公司Oxford Nanopore Technologies(ONT)开发的技术。长读取对于记录基因复制、缺失和其他短读取方法难以捕捉的结构变化非常有价值。重要的是,当需要超快速的响应时,这项技术还可以用于检测其他“组学”指标,比如癌症(见“几分钟的事情”)。
几分钟的事情
超快速测序也可以指导高效的癌症管理。
尽管主要是用于DNA测序的工具,由英国公司Oxford Nanopore Technologies(ONT)开发的平台可以提取其他类型的分子信息,包括基因表达模式和染色体DNA的表观遗传修饰。这些数据可以帮助临床医生加速癌症诊断,使关键的治疗决策在几小时内执行而不是花费数周。
de Ridder领导的团队开发了一个名为Sturgeon的深度学习算法,研究人员使用了从患者DNA甲基化谱中导出的数百万个模拟数据集进行训练。去年,该团队报告说,Sturgeon在仅40分钟的时间内在ONT MinION设备上测序了50个肿瘤样本中的45个,这足够让临床医生在活检过程中患者仍处于麻醉状态时做出治疗决策,并在有需要时直接进行侵袭性手术。该团队还在真实的术中环境中测试了这种方法。de Ridder表示,类似的方法可能对其他异质性肿瘤类型,包括软组织肉瘤,也很有用。
科学家们还在开发基于测序的“液体活检”方法,其中通过检测血液和尿液等体液,可以快速检测、监测和评估癌症的治疗反应。悉尼澳大利亚新南威尔士大学的计算生物学家Martin Smith领导的团队表明,使用MinION进行血样的RNA测序可以将白血病样本的分类时间从几天缩短到几分钟。“Smith表示类似的方法也可以应用于其他时间关键的疾病,包括败血症、感染和自身免疫疾病的爆发。[4]
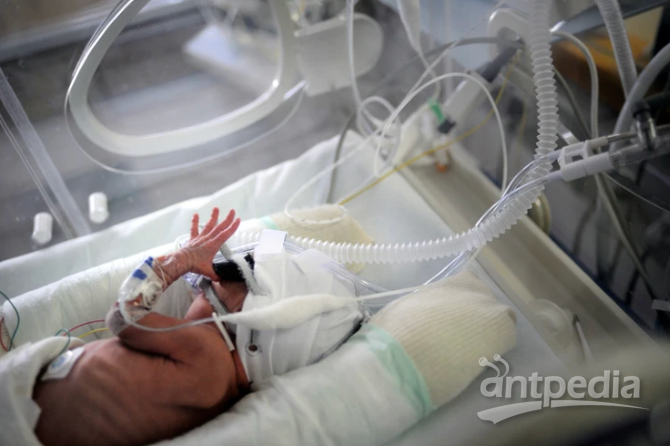
Infants with unknown conditions can benefit from fast diagnoses enabled by rapid sequencing.Credit: Elisabeth Schneider/Look at Sciences/Science Photo Library
展望未来,长读取技术和新型测序平台可能会进一步改变基因组诊断的面貌。然而,除了技术本身,还需要解决一系列人为和后勤问题,如医生的熟悉度、资源分配和公平获得。确保在资源有限地区应用超高速测序技术的挑战将是未来需要解决的难题。总体而言,超高速测序技术的发展为基因组诊断领域带来了革命性的变化,为患者提供了更迅速、个性化的诊断和治疗方案。
Gorzynski, J. E. et al. N. Engl. J. Med. 386, 700–702 (2022).
Vermeulen, C. et al. Nature 622, 842–849 (2023).
Saunders, C. J. et al. Sci. Transl. Med. 4, 154ra135 (2012).
Goenka, S. D. et al. Nature Biotechnol. 40, 1035–1041 (2022).
Sagniez, M. et al. Preprint at medRxiv https://doi.org/10.1101/2022.06.22.22276550 (2022).
三维基因组互作与表观遗传修饰是基因表达调控的重要因素,其动态变化与细胞生长发育及癌症等疾病的发生发展密切相关。解析染色质在活细胞内的时空动态,是理解基因调控机制的重要科学问题。现有基于CRISPR-C......
三维基因组互作与表观遗传修饰是基因表达调控的重要因素,其动态变化与细胞生长发育及癌症等疾病的发生发展密切相关。解析染色质在活细胞内的时空动态,是理解基因调控机制的重要科学问题。现有基于CRISPR-C......
11月1日,在长沙举行的第五届湖南省抗癌协会家族遗传性肿瘤专业委员会学术年会上,中信湘雅生殖与遗传专科医院(下称中信湘雅)首席科学家卢光琇宣布,该院第100位通过胚胎植入前遗传学检测(PGT)技术阻断......
1812年,法国皇帝拿破仑一世从俄罗斯莫斯科撤退时,其大部分军队因饥饿、疾病和寒冷的冬天而损失殆尽。如今,对这撤退途中丧生的30万士兵的部分遗骸的DNA的分析发现,两种未曾预料到的细菌性疾病很可能增加......
1812年夏,法兰西皇帝拿破仑·波拿巴率50万大军入侵俄罗斯帝国。然而到12月时,这支军队仅余零星残部。历史记载将此次“全军覆没”归因于饥寒交迫与斑疹伤寒。但一项新研究表示,从士兵牙齿中提取的DNA,......
美国北卡罗来纳大学研究团队研发出一种名为“DNA花朵”的微型机器人。这种机器人具有独特的自适应环境变化能力,能够像生物体一样,根据周围环境改变形状和行为。“DNA花朵”机器人由DNA与无机材料结合形成......
10月16日,记者从中信湘雅生殖与遗传专科医院获悉,该院研究员林戈、副研究员郑伟团队,联合山东大学、上海交通大学医学院等单位的科研团队开展合作攻关,系统揭示了卵子与早期胚胎质量问题导致女性反复“试管”......
瑞士苏黎世联邦理工学院科学家在最新一期《自然》杂志上发表论文称,他们开发出一款名为MetaGraph的DNA搜索引擎,能快速、高效地检索公共生物学数据库中的海量信息,为研究生命科学提供了强大的专业工具......
究竟是什么让人脑与众不同?美国加州大学圣迭戈分校研究团队发现了一个名为HAR123的小型DNA片段,这将是解开人类大脑独特性之谜的关键。相关研究成果发表于新一期《科学进展》杂志。最新研究表明,HAR1......
衰老对身体产生的可见影响有时与基因活动的无形变化有关。DNA甲基化的表观遗传过程会随着年龄增长而变得不再精确,造成基因表达的变化。而这种变化与随着年龄增长而出现的器官功能衰退和疾病易感性增加有关。如今......