自2012年CRISPR-Cas9技术问世以来,基因编辑便驶入了快车道,取得了一系列新突破。如果将CRISPR-Cas9比作能够破坏目标基因的分子剪刀,那么base editor(碱基编辑器)可以称为分子铅笔,因其能对单个核苷酸进行替换。2019年开发的prime editor则具有更强大的功能,能够对基因组进行搜索和替换,堪称分子世界的“文字处理器”。
开发这些技术的最终目标是修复人类基因中的有害突变。16,000多个小的缺失变异与人类疾病存在因果关系,理论上可以通过插入缺失的序列来修复。囊性纤维化就是一个很好的例子,70%的病例由三核苷酸缺失而引起。
为了实现临床应用,人们需要一种技术来准确、高效且安全地插入序列,避免出现意外的结果。prime editing系统虽然在治疗囊性纤维化等遗传病上表现出巨大潜力,但目前仍不清楚哪些因素决定了编辑效率。
英国Wellcome Sanger研究院和爱沙尼亚塔尔图大学的研究人员近日在Nature Biotechnology杂志上发文称,他们开发出一种新工具,可预测将基因编辑的DNA序列成功插入基因组的几率。

影响插入效率的多个因素
在这项研究中,研究人员试图系统评估插入序列的长度和组成、细胞系、目标位点以及prime editor的不同版本如何影响插入效率。
为此,他们共设计了3,604条pegRNA,编码切口位点上游的插入物,这些插入物的长度从1nt到69nt不等,且GC含量不同。他们将序列插入两个细胞系(HEK293T和HAP1细胞)中,靶向四个目标位点(HEK3、EMX1、FANCF和CLYBL)。一周后,他们对这些细胞进行基因组测序,观察编辑是否成功。评估插入效率的整体策略详见图1。

图1 prime插入效率的高通量测定
由于插入率的变化跨越了三个数量级,于是研究人员试图了解相关的特征,首先是插入物的长度。他们在HEK293T细胞中发现了两个特点:3和4nt序列的插入率高于其他序列;15-21nt序列的插入率高于周围的序列。不过在HAP1细胞中,1-4 nt短序列的插入率并没有高于较长序列。他们将其归因于错配修复(MMR)系统,因为HEK293T细胞在MMR上存在部分缺陷。敲除错配修复基因MLH1的HAP1细胞也证明了这一点,表明MMR系统阻碍了短序列的插入。
之后,他们分析了prime editing的不同步骤如何影响序列的插入率。他们发现,若pegRNA中带有四个或更多的连续腺嘌呤,则插入率会大大下降。此外,prime editing中的另一个重要步骤是带有5’ flap(包含野生型序列)和3’ flap(包含插入物)的中间产物之间达到平衡,而5’ flap核酸酶FEN1及3’ flap核酸酶TREX1和TREX2介导了这种平衡。他们发现,3’ flap核酸酶TREX1和TREX2抑制了较长序列的插入。
同时,插入序列的核苷酸组成和二级结构也会影响插入率。研究人员发现,prime editing系统对胞嘧啶有着明显的偏好。插入序列中每增加1%的胞嘧啶,则插入率平均增加2.2%。相反,腺嘌呤和胸腺嘧啶的百分比则降低了各个位点的插入率。此外,他们还发现,结构强度更高的序列能够被更有效地插入。
在此过程中,他们使用了Twist Bioscience提供的寡核苷酸池。据Twist介绍,他们独特的硅基DNA合成平台能够在单次运行中生成超过一百万条寡核苷酸,对数量几乎没有限制,而且寡核苷酸池精准均一,让人们对实验结果充满信心。此外,实验中使用的多个载体和基因片段也是由Twist Bioscience提供的。
预测不同序列的插入率
在了解影响插入率的多个因素后,研究人员接下来想预测不同序列在同一位点的插入效率。他们采用了机器学习的方法,挑选出10个特征来训练数据,包括插入序列的长度、组成、pegRNA二级结构和MMR等。这种称为MinsePIE的方法能够很好地预测测试数据的插入效率,相关性达到0.68(图2)。
在现有数据上进行训练后,他们在新数据上测试MinsePIE模型,发现它能够准确预测多个插入序列的成功率。之后,他们还对预测的序列进行实验测试。与预测插入率较低的变体相比,预测插入率较高的密码子变体确实表现出较高的插入率,这凸显了MinsePIE模型在密码子优化方面的优势。研究人员认为,这种计算模型可以帮助人们选择出最有效的序列写入基因组中。
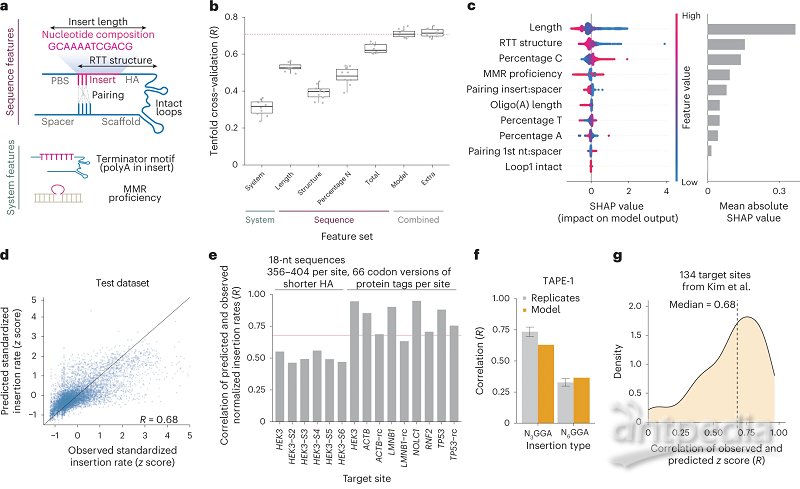
图2 预测prime插入效率
最后,对于如何提高prime editing系统的插入效率,研究人员提出了几点建议。他们建议选择胞嘧啶含量高且容易形成二级结构的序列。对于使用U6启动子的pegRNA,尽量避免腺嘌呤的插入。对于小于14nt的序列,暂时抑制MMR或敲除MLH1将极大提高插入效率。总的来说,这项工作增加了人们对短序列插入效率的理解,有望实现复杂的基因组工程和纠正各种致病突变。
美国科研团队在新一期《自然·生物技术》杂志发表研究成果称,他们基于逆转录酶开发出一种新型基因编辑技术,能够更精准、更高效地同时修复哺乳动物细胞内的多个致病突变,为开发广谱基因疗法奠定了重要基础。许多遗......
随着CRISPR基因编辑技术的不断进步,科学家已将其应用于马、绵羊、猪等动物的遗传改良。英国《自然》网站在日前的报道中指出,经过基因编辑的猪和绵羊等动物,正逐渐在农业领域获得认可。这些技术可提升动物的......
记者27日从中国农业科学院获悉,该院农业基因组研究所农业基因编辑技术研发与应用创新团队构建了全球规模最大的实验验证数据集,并基于此开发出人工智能(AI)大模型AlphaCD。该模型不仅能高效预测超过2......
广州医科大学附属第一医院国家呼吸医学中心主任何建行与合作者在一项研究中发现,一个经过基因工程修饰的猪肺在移植到一名确诊脑死亡的人类患者体内后,能存活9天并发挥功能。研究结果或是跨物种肺移植的首例记录,......
近日,中国农业科学院农业基因组研究所农业基因编辑技术研发与应用创新团队构建了迄今为止规模最大的实验验证数据集,并在此基础上开发了多模态机器学习模型AlphaCD。该模型不仅能够高效预测超过2万种胞嘧啶......
近日,美国哈佛大学与杰克逊实验室联合团队运用先导编辑技术,在小鼠模型中实现了对儿童交替性偏瘫(AHC)致病基因突变的精准修正。此前,中国上海交通大学医学院松江研究院仇子龙教授团队曾证实,全脑碱基编辑技......
瑞典乌普萨拉大学研究团队在6日出版的《新英格兰医学杂志》发表成果称,全球首例由CRISPR-Cas基因编辑技术获得的供体胰岛β细胞,在未使用免疫抑制剂的情况下,在Ⅰ型糖尿病患者体内成功存活,并发挥功能......
神经元中基因编辑的插图。图片来源:杰克逊实验室哪怕在五年前,人们也会认为在活体大脑中进行DNA修复是科幻小说中才有的情节。但现在,科学家已能进入大脑、修复突变,并让细胞在整个生命周期中维持住这种修复效......
美国得克萨斯大学西南医学中心研发的新型基因编辑递送系统,在α-1抗胰蛋白酶缺乏症(AATD)临床前模型上实现了肝脏与肺部的同步靶向治疗。单次给药后,模型症状改善效果可持续数月。这项发表于最新一期《自然......
新一期《自然·通讯》杂志发表一项基因组学重大突破:美国耶鲁大学团队成功将在同一细胞中编辑多个DNA位点的能力提升了2倍,并有效减少了对附近基因位点的非预期突变。新成果使基因编辑的范围和精度同时得以扩大......