ImmunoGen是一家临床阶段的生物技术公司,专注于开发新一代抗体药物偶联物(ADC)以改善癌症患者的预后。近日,该公司宣布,美国食品和药物管理局(FDA)已建议:在铂耐药卵巢癌中开展一项新的单臂研究,可以支持对mirvetuximab soravtansine(IMGN853)的加速批准。
基于这一指导,该公司将启动SORAYA研究,这是一项关键性试验,将评估mirvetuximab soravtansine作为单药疗法在先前接受过Avastin(bevacizumab,贝伐单抗)治疗、叶酸受体α(FRα)高表达、铂耐药卵巢癌患者中的疗效和安全性。
ImmunoGen总裁兼首席执行官Mark Enyedy表示:“我们已经与FDA进行了建设性的讨论,并评估了将mirvetuximab soravtansine更快地应用于患者的所有途径。我们已与FDA达成一致意见,先前接受过贝伐单抗治疗但疾病进展的FRα高表达铂耐药卵巢癌患者需要更好的治疗方案。我们很高兴启动SORAYA研究,在这一患者群体中评估mirvetuximab soravtansine,如果成功,将使我们能够在2021年下半年提交加速审批申请。我们预计,SORAY研究将在下一季度入组首例患者,并预计2021年年中获得顶线数据。”
该公司mirvetuximab soravtansine项目现在包括2个新的试验SORAYA和MIRASOL:(1)SORAYA是一项关键性单臂试验,将入组约100例患者,合格标准包括采用PS2+评分法确认为表达高水平FRα、先前已接受过至多3种方案且至少一种含有贝伐单抗、铂耐药卵巢癌患者。主要终点是研究调查员评估的总缓解率(ORR),关键次要终点是缓解持续时间(DOR)。(2)MIRASOL是一项确认性随机III期试验,430例患者将以1:1的比例随机接受mirvetuximab soravtansine或调查员选择的单剂化疗(每周一次紫杉醇、聚乙二醇化脂质体阿霉素、拓扑替康)。合格标准包括采用PS2+评分法确认为表达高水平FRα、先前已接受过至多3种方案且、铂耐药卵巢癌患者。主要终点是研究调查员评估的无进展生存期(PFS),关键次要终点包括总缓解率(ORR)、总生存期(OS)、患者报告结果。
mirvetuximab soravtansine(IMGN853)是首个叶酸受体α(FRα)靶向ADC,使用一种人源化的FRα结合抗体将ADC专门靶向表达FRα的癌细胞,并使用一种强效抗肿瘤剂DM4杀死所靶向的癌细胞。
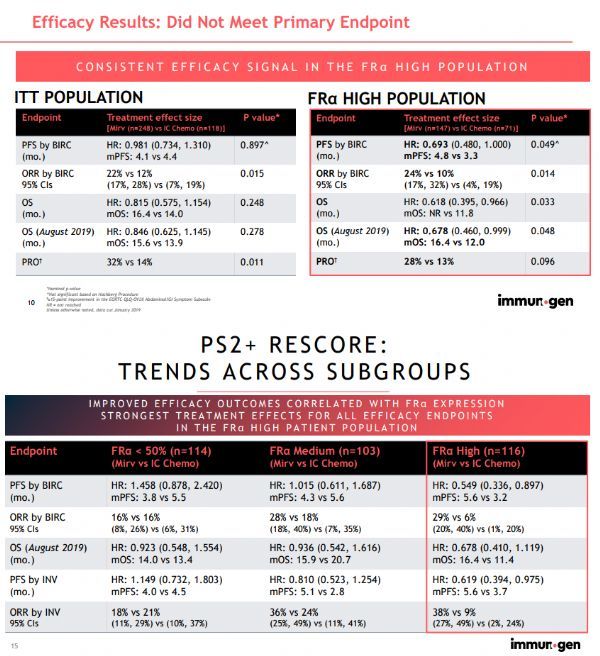
今年3月,ImmunoGen公司公布了mirvetuximab soravtansine治疗FRα阳性、铂耐药卵巢癌III期FORWARD-I研究的结果。显示,研究未能达到主要终点:在整个研究群体中,与化疗相比,mirvetuximab soravtansine未能显著延长PFS。然而,在预先指定的FRα高表达亚组患者中,mirvetuximab soravtansine表现出了令人印象深刻的疗效和耐受性,包括PFS延长(HR=0.69,p=0.049)、ORR提高(24% vs 10%,p=0.014)、OS延长(HR=0.62,p=0.033)。该研究中,mirvetuximab soravtansine的耐受性良好,发生3级或以上不良事件的患者更少(46% vs 61%)、更少的剂量减少(20% vs 31%),因药物相关不良事件导致的停药率更低(5% vs 8%)。
该公司已采用PS2+评分法审查了I期和FORWARD I研究中产生的数据,并确定了70例符合SARAYA关键资格标准的患者。数据显示,在这些患者中的ORR为31.4%(95%CI:20.9%,43.6%)、DOR为7.8个月(95%CI:3.98,-)。这些数据与单用化疗治疗铂耐药卵巢癌的ORR相比相当好,在AURELIA和CORAIL试验中单用化疗的ORR仅为12%,其中包括贝伐单抗初治和经治的患者。
在SORAYA研究中重复出这些数据,将支持在MIRASOL研究完成之前申请加速审批。之后,MIRASOL研究将提供由加速批准转为完全批准所需的随机数据。
聚(ADP-核糖)聚合酶抑制剂(PARPi)在由BRCA1/2和其他DNA修复途径成员突变引起的同源重组(HR)缺陷(HRD)卵巢癌(OC)中具有选择性活性。研究寻求在HR精通细胞中诱导HRD的分子靶......
作为在全球生物制药领域被喻为“魔法子弹”的产品,抗体偶联药物(AntibodyDrugConjugateADC)正迅速崛起为全球创新药领域最受关注的赛道之一。17日,“药明系”第四子药明合联正式在港交......
10月12日,苏州宜联生物医药有限公司(简称“宜联生物”)宣布,已与百欧恩泰(BioNTech)达成战略合作和全球许可协议。双方将合作开发靶向人表皮生长因子受体3(HER3)的下一代抗体偶联药物候选产......
卵巢癌为妇科恶性肿瘤中十分凶险的癌种,被称为“妇癌之王”。据《国家癌症中心:2022年全国癌症报告》显示,我国每年新发卵巢癌患者5.7万,发病率在女性生殖系统恶性肿瘤中位居第3位,死亡率居首位。遗憾的......
卵巢癌的早期筛查终于迎来了好消息!近期,北京大学第三医院的郭红艳/李默团队对219名妇科患者的子宫液进行了代谢组学分析,从中建立了一个由香草扁桃酸、去甲肾上腺素、苯丙氨酸、β-丙氨酸、酪氨酸、12-S......
抗体偶联药物(Antibody-DrugConjugate,ADC)是通过连接子(linker)将具有生物活性的小分子药物偶联至单克隆抗体(单抗)上而产生的。生产用原材料的控制单抗:ADC的单抗生产及......
抗体偶联药物(Antibody-DrugConjugate,ADC)是通过连接子(linker)将具有生物活性的小分子药物偶联至单克隆抗体(单抗)上而产生的。目前绝大部分ADC是由靶向肿瘤抗原的抗体通......
ADC并不是一个具体的药物,而是一类抗体偶联药物。其实一百年前德国化学家PaulEhrlich提出靶向递送细胞毒药物(简单理解杀死肿瘤的药物)的概念,20世纪80年代首次开展ADC药物的临床试验。AD......
卵巢癌是致死率最高的妇科肿瘤,绝大多数患者会经历复发,从铂敏感发展为铂耐药。因此,对于铂类敏感复发的治疗管理尤为重要。近日,复旦大学附属肿瘤医院核医学科主任宋少莉教授团队和复旦大学附属肿瘤医院妇瘤科主......
9月22日,中国国家药品监督管理局已正式批准PARP抑制剂利普卓(奥拉帕利片)新适应症:奥拉帕利联合贝伐珠单抗用于同源重组修复缺陷(HRD)阳性的晚期上皮性卵巢癌、输卵管癌或原发性腹膜癌成人患者,在一......