2018年年初,6名顶尖科学家在《科学》杂志上联名发表题为《基因疗法时代的来临》的文章,回顾了近50年来基因疗法的发展,并对基因疗法的未来表示了乐观的态度并预言下药物发展的下一个阶段将是基因疗法的时代。
随着几个标志性的基因疗法获批, 越来越多的药企加入了这个研发竞争。现在有超越2500个基因疗法正在进行临床试验,值得一提的是,基因疗法现已超越抗体成为现在第二大在研药物类别,仅次于传统的化学药物。

基因疗法面对罕见病有其独有的优势:80%的罕见病是由单基因突变引起的,而传统的疗法只能控制症状,无法触及病因的根本。基因疗法的出现,给罕见病患者带来了治愈疾病的新希望。
1基因疗法的工具箱:载体和平台日趋丰富
工欲善其事,必先利其器。修复“坏掉”的基因,没有趁手的工具是不行的。基因疗法常用的两种治疗手段是 in vivo(体内)和ex vivo (离体)。In vivo像是把修复工具直接注入体内,ex vivo则是把病人的细胞(常为免疫细胞或干细胞)取出来,修好后再给病人回输。而用来传递修复信息的方法,我们称为载体。
载体的种类多种多样,可以分为非病毒类载体和病毒类载体。非病毒载体包括裸露DNA,脂质体或者高聚物包被的DNA,以及多种物理和化学ex vivo的转染技术,机理和使用组织各不相同 。
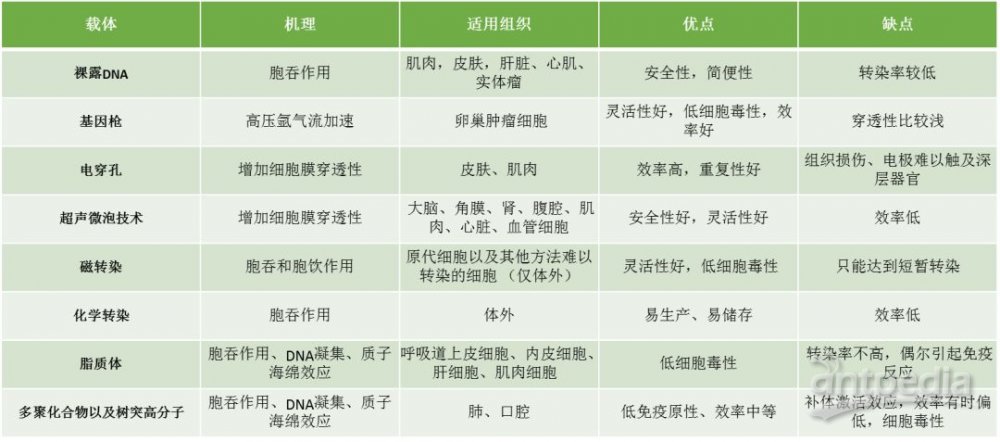
病毒载体则是利用了病毒天然的感染人类的能力,将需要的基因装载到病毒里,投递到细胞或者人体中,而这也是人类驯化这些远比我们古老的微生物的过程。目前使用的病毒载体,诸如腺病毒(AdV)、腺相关病毒(AAV)、单纯疱疹病毒(HSV)、慢病毒等,往往是经过基因改造的病毒,它们变得更温和,急性毒性和遗传毒性都大大降低。这些病毒特性各异,可以根据不同的需求来选择。

病毒载体作为基因补充是非常理想的载体,但是如果想修正错误的基因,病毒载体多少有些力不从心。因此基因编辑平台也被基因疗法寄予厚望。
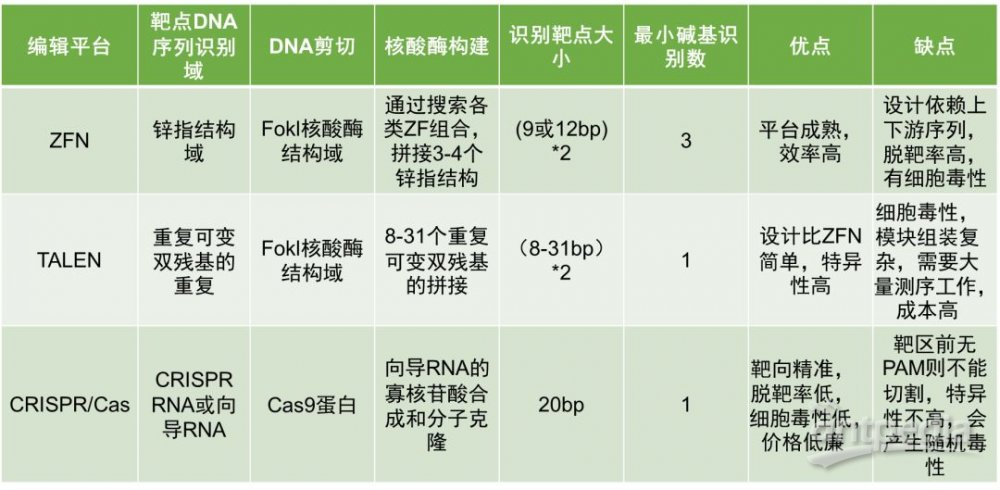
早先科学家使用锌指核酸酶(ZFNs)来编辑基因,但是该技术需要根据不同的序列设计不同的酶,技术门槛高,限制了其实用性。2009年,转录激活因子核酸酶技术(TALENs)诞生,提供了更简单的设计方案。之后的CRISPR/Cas9系统更是让基因编辑得到质的普及。
尽管基因编辑技术还面临一些安全和效率的问题,但这个领域的快速发展还是让科学家和投资人充满信心。
2天价基因疗法能否值回票价?
30万!65万!75万!85万!100万!对,还是美元!
你并非处在一个拍卖场,以上只是现有罕见病基因疗法的报价。药物研发因其高风险高投入,新药价格昂贵可以理解,基因疗法的出现则彻底颠覆了传统药物的定价策略。2016年5月,GSK的Strimvelis (干细胞基因编辑回输疗法) 欧洲获批用于治疗腺苷脱氨酶(ADA)缺乏性重度联合免疫缺陷症(ADA-SCID)批准,定价65万美元。同年9月Sarepta Therapeutics的反义核苷酸药物Exondys51 被FDA批准治疗杜氏肌营养不良症(DMD),该药物花费为每年30万美元。
2017年12月,FDA批准Biogen公司的反义核苷酸药物Spinraza,用于用于治疗成人及儿童脊髓型肌萎缩(SMA), 该药物第一年治疗费用为75万美元,之后每年需要35.5万美元的花费。Spark Therapeutics的Luxuturna也与同月获批,用于治疗由RPE65基因突变引起的视力问题,85万美元的治疗费用只可注射一只眼睛。
然而对患者而言,基因疗法可能是奇迹的出现,生命的转机。患有ADA-SCID的儿童因为先天免疫缺陷,无法对抗病原体的入侵,故只能生活在特制的隔绝塑料罩中,因此被称为“泡泡宝宝”。
GSK的Strimvelis首先从患者的骨髓中取出CD34干细胞,通过转导将一个正常拷贝的ADA基因导入干细胞,然后将干细胞重新导入患者体内,从而在体内产生ADA酶,有望使患者过上正常的生活。该疗法在过去18个患儿身上试验,15名被完全治愈。
SMA是一种罕见遗传病,患者出生就患有基因突变引起的神经元丧失,导致无法控制肌肉运动,最终肌肉萎缩,失去行动甚至呼吸的能力。2014年Camille的父母发现她无法直立,随后被诊断为SMA。在接受了Spinraza的治疗以后,Camille的病情得到了良好的控制,甚至可以自由走动,并在脸书上更新自己的治疗状态。
3结言
面对罕见病基因疗法的定价,我们似乎无法用传统的药物定价策略来衡量。天平的两端,一端是药物研发的可持续性发展,另一端是患者的强烈需求,如何平衡,很多时候只能交给市场。另一款UniQure公司获批的基因疗法Glybera,因为在欧洲100万美元的定价少有人问津而黯然退出市场。尽管如此,越来越多基因疗法的成功定将使患者受益。
国内罕见病政策的一路绿灯,势必会刺激新一波的研发热情,而海外成熟基因疗法的引进则是最快速度造福患者的捷径。9月,美柏医健,携手海外最前沿的基因疗法企业,在波士顿等您,一起迎接这场2018年生物技术的盛宴!
参考资料:罕见病基因疗法产业图谱


本期作者:任晓远
本科毕业于北京大学药学院,于瑞典卡罗林斯卡医学院获得硕士和博士学位。现就职于卡罗林斯卡医学院,从事抗肿瘤和抗生素药物研发相关课题,长期关注医药行业研发动态,同时担任北欧华人创新创业协会秘书长。现任美柏医健研究员。
南非更新了国家健康研究伦理指南,其中增加了关于可遗传人类基因组编辑的新章节。研究人员对此表示担忧。受精后5至9天、处于囊胚阶段的人类胚胎图。图片来源:JuanGaertner/SciencePhoto......
近日,生物工程学院智能生物制造教育部重点实验室基因编辑与合成生物工程课题组刘嵘明教授受邀在生物工程领域国际权威Top期刊《生物技术发展趋势》(TrendsinBiotechnology)发表题为“在工......
第七届进博会7日正在上海举行。跨国企业展台展现了对罕见病治疗的关注。武田制药携全新“罕见出凝血创新药家族”集体亮相进博会舞台。该“家族”成员包括多款变革性治疗药物与创新疗法,比如:治疗获得性血友病的注......
北京市卫生健康委日前公布2024年罕见病药品保障先行区医疗机构“白名单”。北京协和医院、北大医院、北京儿童医院、首儿所、宣武医院、北医三院、天坛医院、北大人民医院、积水潭医院、解放军总医院第一医学中心......
生物法合成NMN有新突破。据中国科学院天津工业生物所消息,该所通过开发从头合成途径提高烟酰胺单核苷酸(NMN)产量,实现超过100倍的NMN产量提升。报道称,天津工业生物技术研究所通过系统工程化改造大......
图二甲双胍逆转灵长类多维衰老时钟在国家自然科学基金项目(批准号:81921006、92168201、92149301)等资助下,中国科学院动物研究所刘光慧研究员与曲静研究员团队联合中国科学院北京基因组......
近日,引正基因宣布完成战略融资,由戈壁大湾区旗下管理的AEF大湾区创业基金投资。引正基因是一家精准基因组编辑技术解决方案提供商,是基因编辑平台型技术公司,专注基因编辑工具底层技术开发。公司开发的基于C......
关于公开征求《罕见病药物临床药理学研究技术指导原则(征求意见稿)》意见的通知为科学指导和规范罕见病药物的临床药理学研究与评价,促进罕见病药物的研发,我中心组织起草了《罕见病药物临床药理学研究技术指导原......
关于公开征求《模型引导的罕见病药物研发技术指导原则(征求意见稿)》意见的通知为指导在罕见病药物研发过程中科学合理设计定量药理学研究以及有效应用定量药理学方法,提高罕见病药物研发效率,我中心组织起草了《......
10月4日港股开盘后,药明系股价飙涨。截至中午发稿,药明康德(2359.HK)股价大涨超过13%,药明生物(2269.HK)大涨超过12%。药明系企业股价大涨与一份券商发布的报告有关。里昂证券发布的一......